Tabelul periodic al elementelor chimice a împlinit 150 de ani
Tabelul periodic al elementelor chimice poate fi văzut în toate laboratoarele de chimie. Meritul pentru crearea acestuia este atribuit, în general, lui Dmitri Mendeleev, un chimist rus care, în anul 1869, a aranjat cele 63 de elemente chimice cunoscute la acea vreme pe rânduri și coloane în funcție de proprietățile lor chimice și fizice.
Pentru a sărbători cea de-a 150-a aniversare a acestui moment crucial din știință, ONU a proclamat anul 2019 drept Anul Internațional al Tabelului Periodic al Elementelor.
Tabelul periodic al elementelor nu a început însă cu Mendeleev. Mulți alţi chimişti au încercat să găsească o modalitate de aranjare a elementelor chimice în funcţie de proprietăţile lor.
Cu zeci de ani înainte de Mendeleev, chimistul John Dalton a realizat un tabel cu elementele chimice cunoscute la acea vreme și a utilizat câteva simboluri destul de interesante pentru acestea.

Lista elementelor chimice a lui John Dalton. Credit: Wikimedia.
De asemenea, cu câțiva ani înainte de Mendeleev, John Newlands a creat un tabel în care a ordonat elementele chimice în ordinea maselor atomice relative.
În anul 1865, John Newlands a publicat Legea Octavelor aranjând toate elementele cunoscute la acea vreme, începând cu H (hidrogen) și terminând cu Th (thoriu), în opt grupuri de câte opt, pe care acesta le-a asemănat cu octavele din muzică.
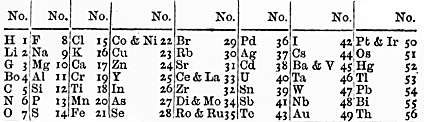
Tabelul elementelor al lui John Newlands. Credit: Wikipedia.
Geniul lui Mendeleev a constat în faptul că el a înţeles că anumite elemente chimice lipsesc din tabele şi că acestea urmează să fie descoperite.
Spre deosebire de Dalton, Newlands și alți chimişti care au inclus în tabelele lor doar elementele chimice cunoscute, Mendeleev a lăsat spații libere pentru elementele chimice necunoscute. Chiar mai uimitor, el a prezis cu acuratețe proprietățile elementelor chimice necunoscute.

Tabelul lui Dmitri Mendeleev completat cu elementele chimice necunoscute. Credit: Wikimedia Commons
Observați semnele de întrebare din tabelul de mai sus?
De exemplu, lângă Al (aluminiu) există un spațiu pentru un metal necunoscut. Mendeleev a prezis că acesta va avea masa atomică 68, densitatea de 6 g/cm3 și un punct de topire foarte scăzut.
Șase ani mai târziu, Paul Émile Lecoq de Boisbaudran a izolat elementul chimic Ga (galiu) care are masa atomică 69,7, densitatea de 5,9 g/cm3 și un punct de topire atât de mic încât devine lichid în palmă, deoarece punctul de topire al galiului este la 29,7646 °C.
În acelaşi mod Mendeleev a prezis elementele chimice Sc (scandiu), Ge (germaniu) și Tc (technețiu), care a fost descoperit abia în anul 1937, după 30 de ani de la moartea lui Mendeleev.
La prima vedere, tabelul lui Mendeleev nu seamănă prea mult cu tabelul periodic al elementelor chimice pe care îl utilizăm în prezent. Acesta din urmă cuprinde o mulţime de elemente pe care Mendeleev le-a ignorat și pentru care nu a lăsat loc liber, mai ales gazele nobile, cum ar fi He (heliu), Ne (neon), Ar (argon).
Mai mult, tabelul lui Mendeleev este orientat diferit faţă de tabelul modern al elementelor chimice.
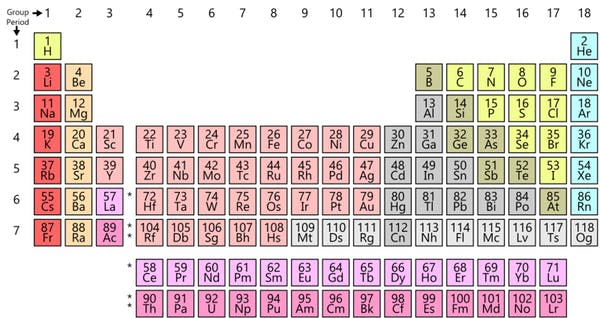
Tabelul modern al elementelor chimice. Credit: Offnfopt/Wikipedia.
De îndată ce rotiţi tabelul lui Mendeleev cu 90 de grade, similitudinea acestuia cu versiunea modernă devine evidentă.
De exemplu, halogenii, F (fluor), Cl (clor), Br (brom) și I (iod), simbolizat J în tabelul lui Mendeleev, se grupează unii sub alţii şi formează coloana sau grupa a 17-a din tabelul actual al elementelor chimice.
Perioada de experimentare
Diferenţa dintre tabelul lui Mendeleev şi versiunea modernă a tabelului periodic al elementelor chimice ar putea părea nesemnificativă, dar, după doar câțiva ani de publicarea tabelului lui Mendeleev, au apărut o mulțime de variante ale acestuia.
Chiar înainte ca tabelul lui Mendeleev să fie rotit cu 90 de grade, precum în versiunea modernă, chimiştii au propus câteva moduri ingenioase de aranjare a acestuia.

Spirala elementelor chimice a lui Heinrich Baumhauer. Credit: American Chemical Society.
Un exemplu frapant îl reprezintă spirala lui Heinrich Baumhauer, care a fost publicată în 1870, având hidrogenul în centrul său și elementele chimice grupate, în spirală, în ordinea creşterii masei atomice.
Elementele de pe fiecare din „spițele” aceste „roți” au proprietăți identice, la fel precum elementele din aceeaşi coloană (grupă) a tabelului periodic al elementelor chimice din prezent.
Formatul orizontal al tabelului elementelor chimice a apărut la începutul secolului al XX-lea odată cu versiunea propusă de Alfred Werner în anul 1905.
Pentru prima dată, gazele nobile se aflau în poziția lor binecunoscută de la marginea din dreapta a tabelului.
Werner s-a inspirat din lucrarea lui Mendeleev, lăsând spaţii goale pentru elementele chimice despre care bănuia că există, deși a sugerat posibilitatea existenţei unor elemente chimice mai ușoare decât hidrogenul și a unui element între hidrogen și heliu care în realitate nu există.
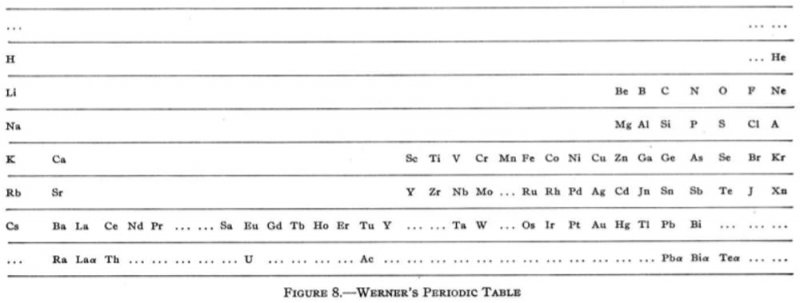
Tabelul elementelor chimice al lui Alfred Werner. Credit: American Chemical Society.
O altă versiune deosebit de importantă a tabelului elementelor chimice a fost cea propusă de Charles Janet. Acesta a folosit fizica cuantică pentru a crea un tabel periodic al elementelor chimice bazat pe configurația electronică a elementelor.
Tabelul lui Charles Janet este încă preferat de mulți fizicieni. Interesant, Janet a lăsat, de asemenea, spaţii libere pentru elementele chimice cu numărul atomic până la 120, în ciuda faptului că la acea vreme erau cunoscute doar 92 de elemente chimice.
În prezent numărul elementelor chimice cunoscute este 118.

Tabelul elementelor chimice al lui Charles Janet. Credit: Wikipedia, CC BY-SA
Stabilirea unui format
Versiunea modernă a tabelului periodic al elementelor chimice este de fapt o evoluție directă a versiunii lui Charles Janet.
Metalele alcaline, grupul de elemente chimice care începe cu Li (litiu), precum și metalele alcalino-pământoase, grupul de elemente chimice care începe cu Be (beriliu), au fost mutate de la marginea din dreapta a tabelului lui Janet la marginea din stânga pentru a crea un tabel periodic cu un aspect foarte larg (wide).
Problema cu acest format este că nu se potrivește foarte bine pe o pagină sau un poster.
Din motive estetice, elementele chimice din blocul f sunt de obicei mutate sub tabelul principal. Așa am ajuns la formatul actual al tabelului periodic al elementelor chimice.
Aceasta nu înseamnă că nu au mai fost propuse şi alte formate ale tabelului elementelor chimice, de multe ori pentru a evidenția unele corelații dintre elementele chimice care nu sunt ușor de remarcat în tabelul convențional.
În prezent există sute de variante ale tabelului periodic al elementelor chimice, aşa cum se poate constata din baza de date a lui Mark Leach, spiralele și versiunile 3D fiind deosebit de populare.
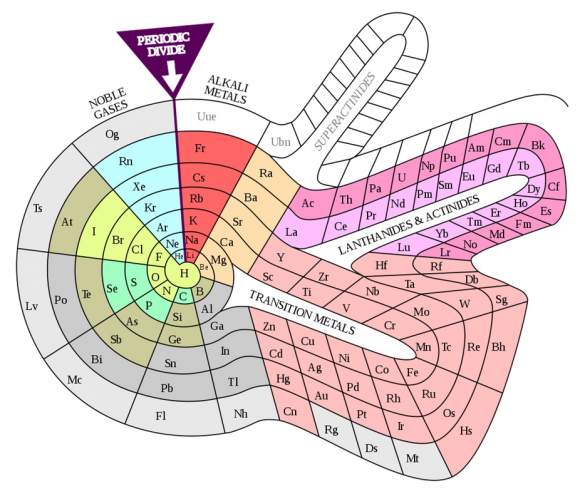 Spirala elementelor chimice a lui Theodor Benfey (1964). Credit: DePiep/Wikipedia
Spirala elementelor chimice a lui Theodor Benfey (1964). Credit: DePiep/Wikipedia

„Floarea lui Mendeleev”. O versiune 3D a tabelului periodic al elementelor. Credit: Тимохова Ольга/Wikipedia, CC BY-SA
Toate aceste versiuni arată modul prin care tabelul periodic al elementelor chimice a devenit simbolul științei.
Traducere şi adaptare după The periodic table is 150 – but it could have looked very different